Reglas para calcular valencias
enero 06, 2022La valencia es una medida de la reactividad de un átomo o molécula. Puedes obtener la valencia de varios elementos mirando sus posiciones en la tabla periódica, pero no de todos. También es posible calcular la valencia de un átomo o molécula observando cómo este/a se combina con otros átomos o moléculas de los cuales conocemos la valencia.
Regla del octeto
Al determinar la valencia de un átomo o molécula (para aquellos que no puedan analizarse usando la tabla periódica), los químicos utilizan la regla del octeto. Según esta regla, los átomos y sustancias químicas se combinan de tal manera de tener ocho electrones en la capa externa de cualquier compuesto estén formando. Una capa externa con ocho electrones está llena, lo que indica que el compuesto es estable.
La tabla periódica
Los científicos han organizado todos los elementos que conocemos en una gráfica conocida como la tabla periódica y, en muchos casos, la valencia está a simple vista en la misma. Por ejemplo, todos los metales en la columna 1, incluyendo el hidrógeno y el litio, tienen una valencia igual a +1; todos aquellos en la columna 17, incluyendo el flúor y el cloro, tienen una valencia igual a -1. Los gases nobles en la columna 18 tienen una valencia igual a 0 y son inertes.
Determinando la valencia mediante formulas químicas
Se puede determinar la valencia de un elemento de transición o un radical en un compuesto observando cómo es la combinación con elementos de valencia conocida. Esta estrategia está basada en la regla del octeto, que nos dice que los elementos y radicales se combinan de tal manera de producir una capa externa estable de ocho electrones.
Como demostraciones sencillas de esta estrategia, nótese que el sodio (Na), con una valencia de +1, se combina fácilmente con el cloro (Cl), que tiene una valencia de -1, para formar cloruro de sodio (NaCl) o sal de mesa. Este es un ejemplo de una reacción iónica en la que un electrón es donado por un átomo y recibido por el otro.

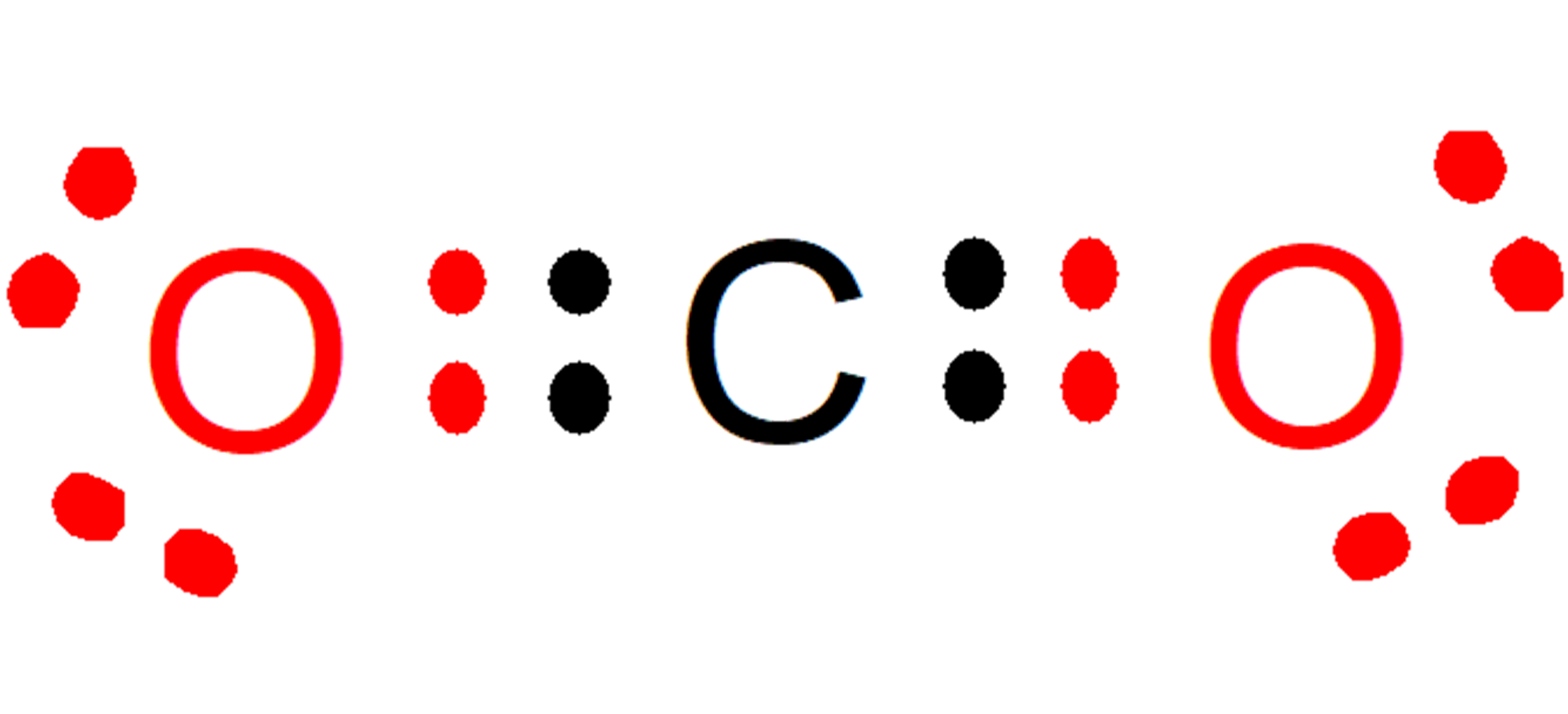



0 comments